我校马萍教授团队融合多组学与类器官/器官芯片技术
取得系列高水平研究成果
我校环境风险与相关疾病精准防控湖北省重点实验室马萍教授团队,深耕多组学与类器官/器官芯片两大核心技术的交叉融合研究,成功实现“环境暴露-分子机制-疾病效应”的精准关联。近两年,团队相关研究成果持续发表于中科院大类1 区 SCI 期刊,累计达11篇,为环境风险评估、毒性机制解析及天然产物防护研发提供了重要的科学支撑与技术参考。
类器官与器官芯片是当下生命科学领域的前沿技术:类器官通过体外三维培养技术构建,可高度还原人体器官的组织结构、生理功能与病理反应;器官芯片依托微流控与组织工程技术,在芯片上重建器官生理结构、血流动力学及细胞间相互作用,是精准模拟人体器官生理病理过程的创新模型。马萍教授团队立足两大技术优势,成功构建基于HepG2细胞的三维肝脏类器官和肝脏器官芯片平台,针对镉(Cd)、食品包装污染物邻苯二甲酸二丁酯(DBP)的肝毒性机制及防护策略开展系统性探索,四项创新性研究成果相继发表于中科院大类 1 区 TOP 期刊,研究水平与应用价值获业内高度认可。
镉污染是威胁全球粮食安全的重大环境问题,补硒虽被广泛用于缓解镉毒性,但其安全使用范围始终存在争议。马萍团队2026年1月在中科院1区Top期刊《npj Science of Food》发表的《Application of HepG2-derived organoid and organ-on-a-chip platforms in elucidating selenium-mediated protection against cadmium-induced liver dysfunction》研究中,首次借助肝类器官与器官芯片模型,清晰揭示了硒浓度与镉毒性保护效应之间的复杂剂量关系。研究发现,镉暴露会呈剂量依赖性引发肝损伤,低浓度硒可有效缓解镉诱导的氧化应激、炎症反应及肝功能指标异常;而高浓度硒不仅会丧失防护作用,反而会加剧镉诱导的肝细胞代谢紊乱与氧化损伤。该研究为公众科学认知富硒食品、合理使用硒补充剂提供了直接实验证据,警示盲目高剂量补硒可能适得其反,也为制定精准的膳食硒摄入指南贡献了关键科学依据。该论文由马萍教授与中国疾病预防控制中心苏丽琴研究员共同担任通讯作者,我校 2022 级硕士生任梦为第一作者。
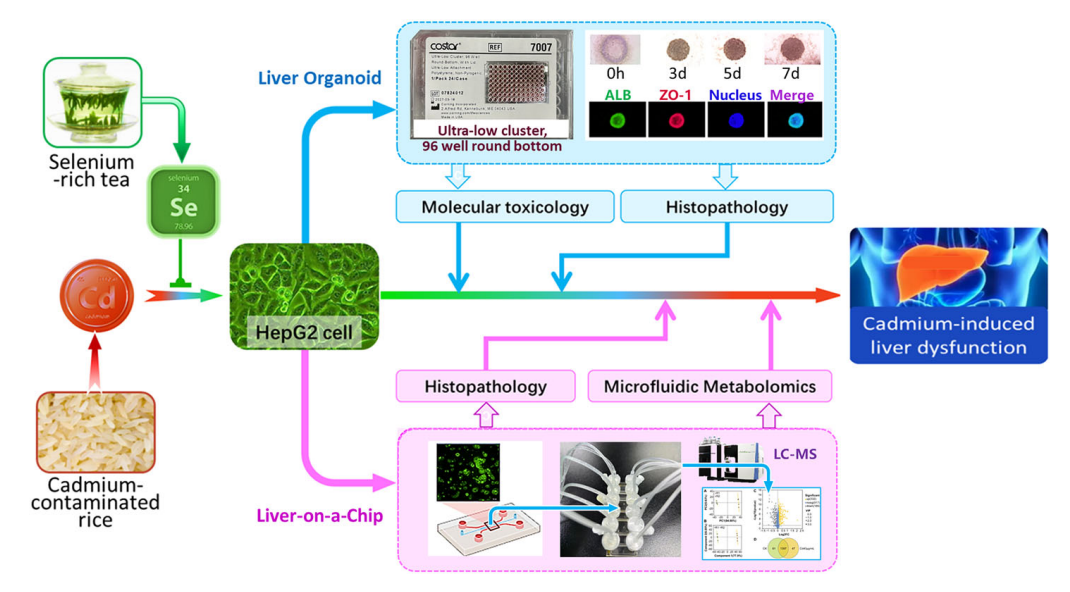
图1 论文科学假说图
针对食品包装中广泛存在的增塑剂邻苯二甲酸二丁酯(DBP),马萍团队同步开展机制解析与天然产物干预双线研究,取得系列突破性成果。团队率先利用肝脏类器官和肝脏器官芯片平台,精准解析出DBP致肝损伤的核心分子通路:DBP 通过诱发氧化应激(激活Nrf2/NF-κB通路)与引发脂质代谢紊乱(抑制 PPAR-α通路)的双重作用,协同造成肝细胞损伤。同时,研究证实常见抗氧化剂维生素C可有效逆转上述通路异常,显著缓解DBP所致肝毒性,为经典护肝策略提供了全新的分子机制佐证。成果《HepG2 three-dimensional cellular models and omics analysis: the mechanisms of DBP-induced liver dysfunction》2025年9月发表于中科院1区 Top 期刊《Food Science and Human Wellness》,马萍教授为通讯作者,我校 2022 级硕士生冯庆与鲁素蕊老师为共同第一作者。
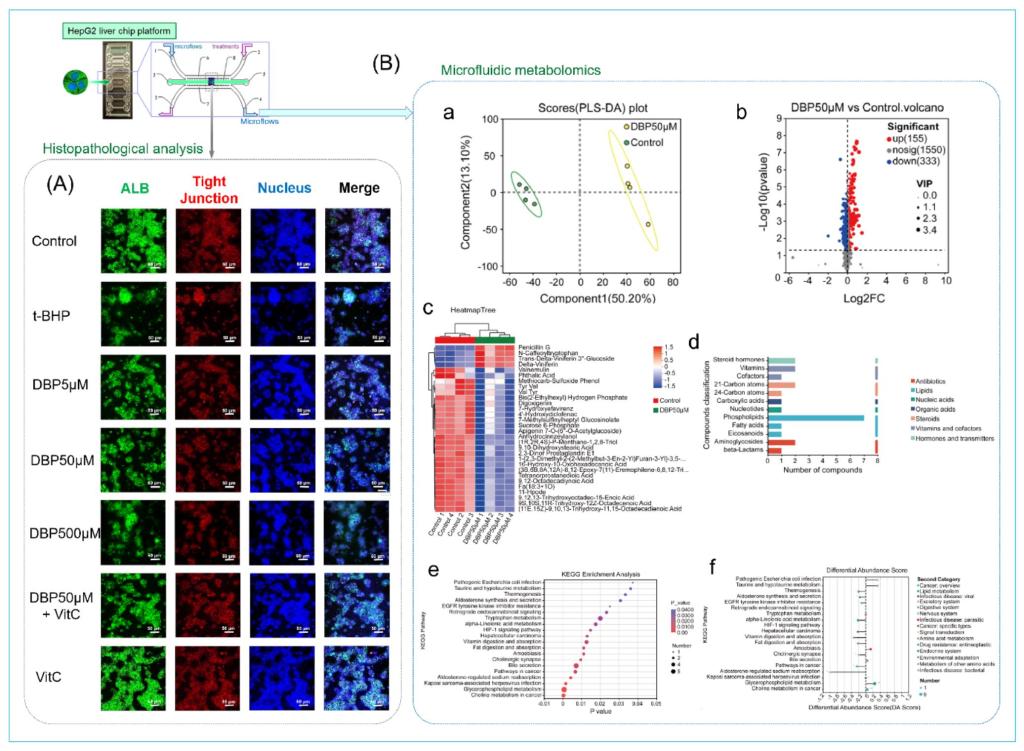
图2肝脏器官芯片的免疫荧光图像和流出液的代谢组学结果
在明晰DBP肝毒性机制的基础上,团队进一步从天然植物中挖掘高效防护方案,取得重要创新进展。研究发现,桂花水提物能显著拮抗DBP诱导的肝损伤,其活性成分可高效结合并激活Nrf2、PPAR-α等关键靶点,同步缓解氧化应激与脂质代谢紊乱,从根源上改善DBP所致的肝细胞损伤。该研究为开发基于天然产物的肝损伤防护产品开辟了全新路径,也为“药食同源”理念在食品安全防护领域的应用提供了新思路。成果《Protective effect of osmanthus water extract on liver dysfunction caused by DBP based on organoids and organ chips technologies》2025年7月发表于中科院1区Top期刊《Food Research International》,由马萍教授与鲁素蕊老师共同担任通讯作者,我校2022级硕士生冯庆为第一作者。
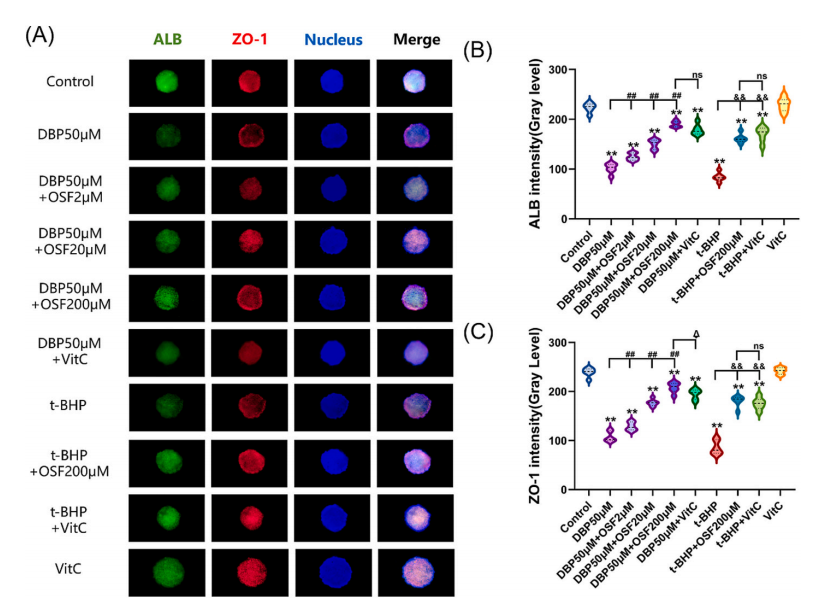
图3 HepG2肝类器官的免疫荧光染色图像
微塑料已成为全球性新型污染物,广泛分布,可通过食物链逐级富集,对生态系统与人体健康构成多重威胁。它难以降解、易吸附重金属与有毒有机物,进入人体后可在肠道、血液、脏器累积,引发慢性炎症、干扰内分泌、损害肠道屏障,还可能增加心血管、神经与呼吸系统疾病风险,是当前环境健康领域亟待防控的重要隐患。马萍团队开展了微塑料加重过敏性哮喘的机制研究,2026年1月,在环境领域中科院1区Top期刊《Environment International》发表题为《Gut-lung axis: a novel mechanism involving microbiota dysbiosis-coordinated PLA2-TRPV1 neuroimmune crosstalk in nanoplastic-induced asthma exacerbation》的研究论文,系统揭示了20 nm聚苯乙烯纳米塑料(PS-NPs)加重过敏性哮喘的分子机制。研究基于OVA致敏小鼠模型,综合气道高反应性检测、肺组织病理学分析、免疫组化、多组学技术等手段,首次提出“肠-肺轴”介导的代谢-免疫-神经炎症调控网络新机制。结果表明,PS-NPs暴露可激活肺组织磷脂酶A2(PLA2)通路,促进花生四烯酸代谢物积累,上调TRPV1通道表达并诱导神经SP和CGRP释放,形成PLA2–TRPV1神经免疫正反馈环路,显著增强NF-κB信号通路活化及Th2型炎症反应。同时,PS-NPs导致肠道菌群失衡,增加可产生六酰化LPS的革兰氏阴性菌丰度,破坏肠道屏障结构,通过TLR4/NF-κB信号轴放大肺部炎症反应。多组学整合分析进一步证实,代谢重编程与微生物紊乱协同驱动气道炎症与高反应性加重。该研究从“微生物—代谢—神经—免疫”多维度系统阐明了纳米塑料加重哮喘的关键机制,为评估新兴污染物呼吸毒性风险及寻找潜在干预靶点提供了重要理论依据。
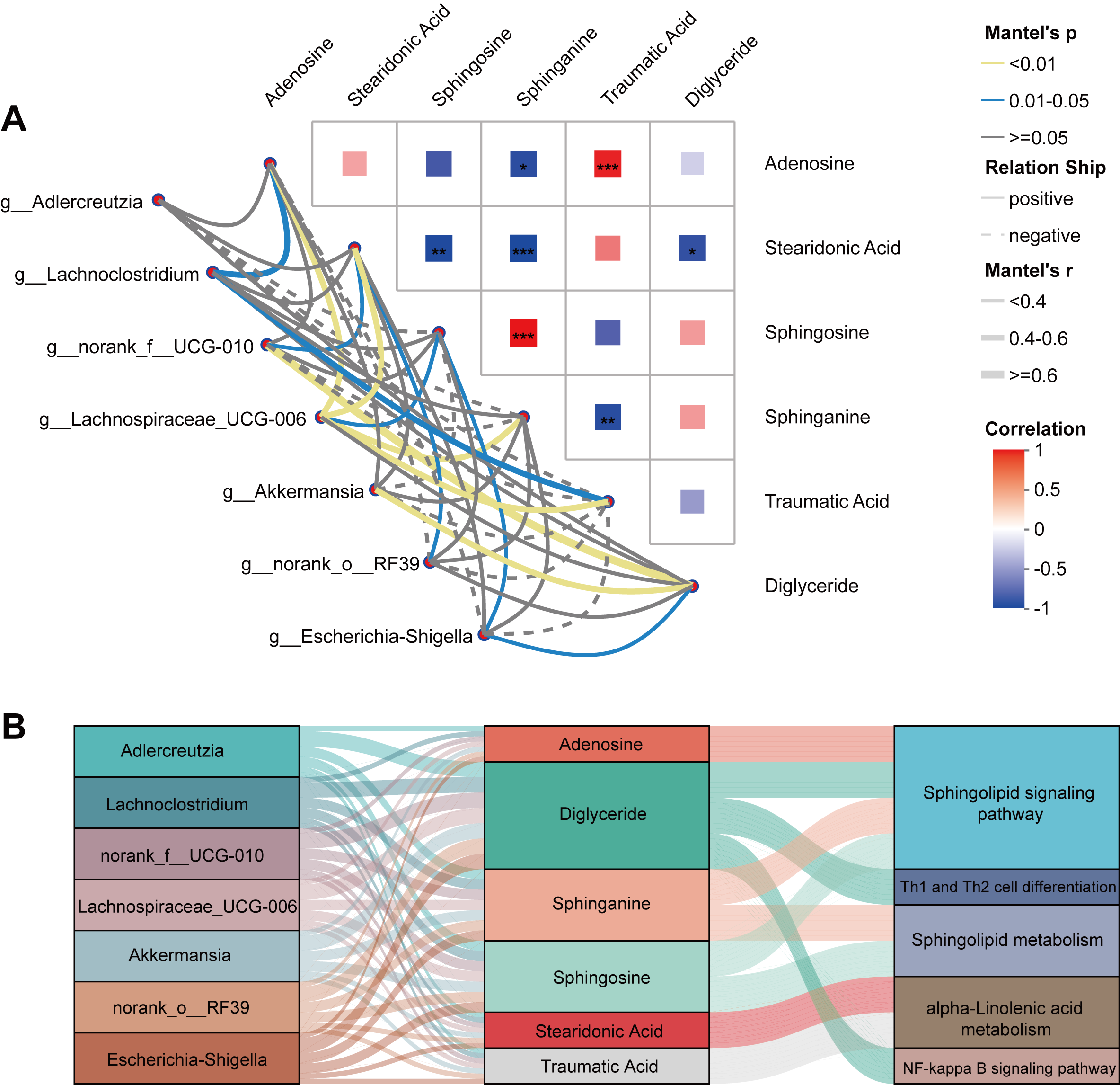
图4 微生物组学和肺部代谢组学的联合分析
据悉,该系列研究均由我校环境风险与相关疾病精准防控湖北省重点实验室独立完成,获得国家自然科学基金面上项目、湖北省卫健委重点支撑项目及我校科研创新团队项目的联合资助。马萍教授表示,此次系列成果不仅深化了学界对镉、DBP、微塑料等典型污染物肝、肺毒性分子机制的理解,更充分展现了多组学和类器官/器官芯片技术在环境风险评估、毒理学机制研究和天然产物开发中的巨大应用潜力。未来,团队将持续推进该前沿技术的标准化与产业化应用,聚焦公共健康保障需求开展更多针对性研究,为环境风险与疾病防控领域贡献更多“湖科智慧” 与“湖科方案”。